主動跨前服務,區市場監管局助力企業醫療器械產品上市
前不久,位於新河富盛開發區的明基三豐醫療器材(上海)有限公司的手術台取得了第二類醫療器械注冊証。這意味著,企業的醫療器械產品離落地投產又加快了一大步。“這多虧了崇明區市場監督管理局給予我們企業及時、有效的幫助,讓產品注冊周期比預期縮短了半年,大大加快了我們產品上市的時間。”明基三豐醫療器材(上海)有限公司企業業務部經理陳俊宏激動地表示。
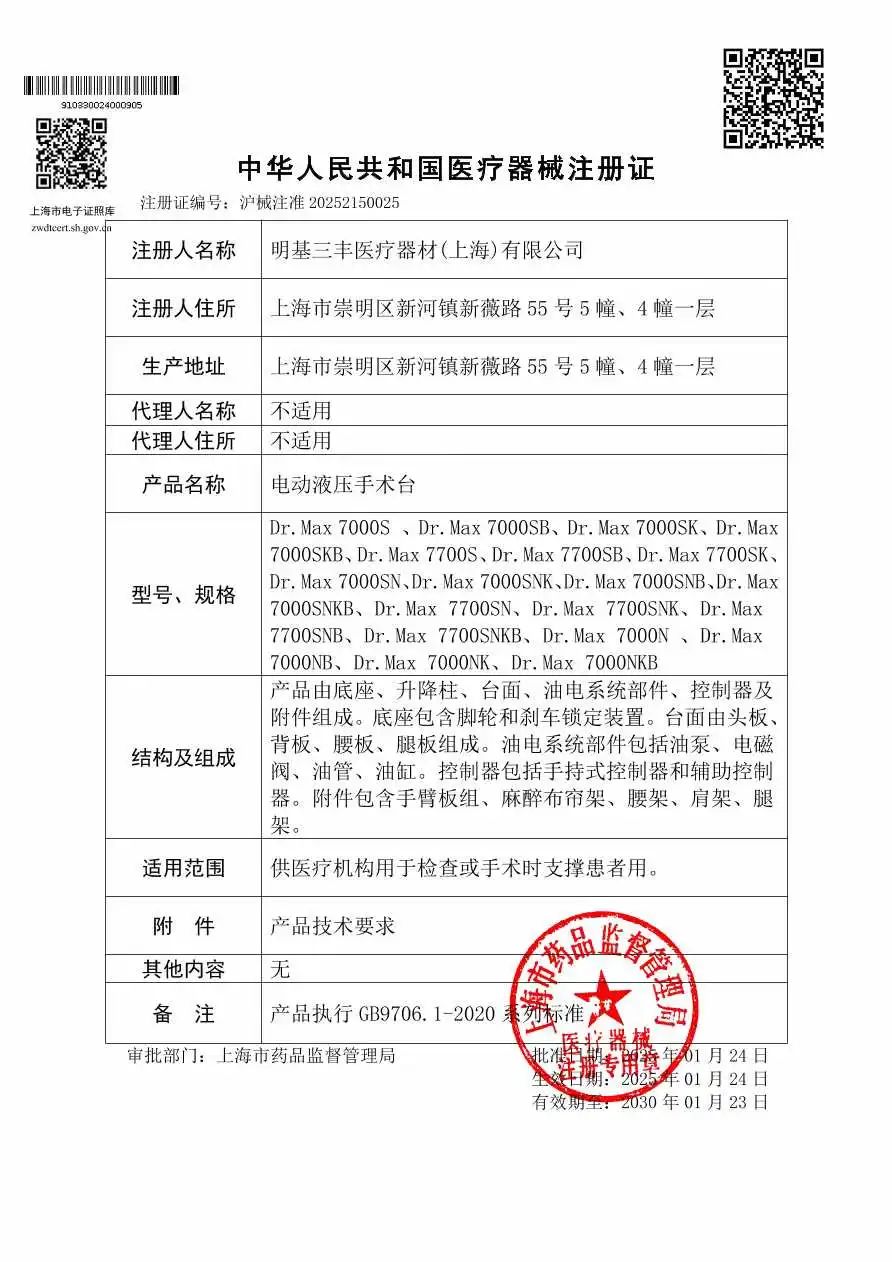

據了解,該企業隸屬於世界五百強的中國台灣明基(BenQ)集團,主要生產手術室必備設備——手術燈、手術床及吊塔與一體化手術室解決方案等系列產品,迄今已在國內市場銷售20多年。產品在中國手術室醫療設備市場的佔有率為全國第四名,產品受國內多家三甲醫院信賴及認可。
為了擴大產業規模,該企業決定將生產線搬至大陸,於2024年在新河富盛開發區建立生產基地。企業進駐后不久,區市場監管局便主動跨前,積極問需,及時回應和解決企業關切及訴求。去年年中,企業多款醫療器械擬申請第二類醫療器械產品注冊証,該証是醫療器械的“合法身份証”,証明產品依照法定程序,通過了監管部門對其安全性、有效性的系統評價,准予投入生產並上市銷售,是研發成果轉化上市的重要一步。“我們來自中國台灣,又是首次在大陸初創的企業,對當地的產品注冊需要的審批手續、操作流程不熟悉,難免會遇到磕磕絆絆。好在這個過程中,區市場監管局為我們出主意想辦法,提供了專業、高效的指導,打消了我們的顧慮,少走很多彎路。”陳俊宏介紹,區市場監管局相關人員帶領企業員工赴市醫療器械化妝品審評核查中心(簡稱市器審中心)進行申報前的產品注冊咨詢。經過現場“把脈問診”后,市器審中心從多方面為企業提供了具體的、有針對性的指導意見。在多方的支持下,輔導企業完善申請材料。

不僅如此,在后續的現場審評過程中,區市場監管局還全程陪同市器審中心檢查組對企業開展現場核查,面對檢查組提出的疑問,及時幫助企業提供准確的解釋和補充說明,針對檢查中出現的缺陷項,將缺陷產生背景、核查組關注重點情況傳達給企業。在審評結束后,還持續關注企業的整改情況,定期與企業溝通,了解整改措施的執行進度。“這個過程中,我們特別感謝區市場監管局,在他們的指導下,我們聯系了第三方檢測機構,讓他們上門對我們的醫療器械進行檢驗,省去了我們來回奔波的麻煩,這樣的服務太貼心了。”陳俊宏坦言,“沒想到我們能在這麼短的時間就取得了注冊証,我相信在區市場監管局的幫助下,很快將拿到投產前的最后一証——生產許可証,預計將於3月中旬開始投產。”
(來源:上海崇明)
分享讓更多人看到 
- 評論
- 關注



























 第一時間為您推送權威資訊
第一時間為您推送權威資訊
 報道全球 傳播中國
報道全球 傳播中國
 關注人民網,傳播正能量
關注人民網,傳播正能量